TMB的出现及发展
TMB 基本现状
定义
- WES:
TMB是指肿瘤基因组内存在的体细胞突变位点数量,可以间接反映肿瘤产生新生抗原的能力。由于早期研究多基于WES检测,因此TMB通常是指单位基因组外显子编码区域(外显子组,exome)的突变数量(mutations, muts),单位为muts/exome。
- Panel:
虽然WES是检测TMB的金标准,但WES时间成本和分析成本较高。经过多项大样本研究验证后,TMB检测从WES扩展到了更切合临床实际的靶向二代测序(next-generation sequencingpanel, NGS panel)。靶向测序的基因检测位点比外显子组少,由于不同平台检测方法和测序覆盖的外显子区域长度不同,TMB也被定义为肿瘤基因组区域中每兆碱基(megabase, Mb)发生的碱基替换突变和插入缺失突变的数量总和,单位为muts/Mb。
纳入计算的突变范围
- WES
TMB被定义为通过WES测序肿瘤组织样本中体细胞非同义突变数量的总和。
- Panel
在NGSpanel检测TMB的研究中,纳入TMB计算的是体细胞编码区中碱基替换突变和插入缺失突变,部分NGS panel计算TMB也同时纳入了同义突变,而胚系变异、核苷酸多态性位点、明确的抑癌基因及驱动基因热点突变则不计算在内.(Analysis of 100,000 human cancer genomes reveals the landscape of tumor mutational burden、The COSMIC (Catalogue of Somatic Mutations in Cancer) database and website、ExAC:Analysis of protein-coding genetic variation in 60,706 humans )
TMB计算过程中分母的选择-2023年9月补充
实际在进行TMB计算过程中,尤其是使用Panel进行捕获的产品,分母的选择也是成为了困扰。部分机构会直接使用Panel的全长(涵盖内含子之类的区域)作为分母进行计算,但是还有一些机构会选择使用编码区域全长作为分母。所以在这里也记录看到的一些处理方式以供参考。
- 使用编码区长度
FoundationOne®CDx June 7, 2022 技术文档中提到,
The resulting mutation number is then divided by the coding region corresponding to the number of total variants counted;其实略尴尬,TMB共识普遍建议应该使用的Panel(当然未明确说明编码区和内含子区域的比例)在1MB以上,但是FoundationOne的编码区大小仅753kb。[肿瘤突变负荷应用于肺癌免疫治疗的专家共识] TMB 定义中提到,
由于早期研究多基于WES检测,因此TMB通常是指单位基因组外显子编码区域(外显子组,exome)的突变数量(mutations, muts),单位为muts/exome。虽然WES是检测TMB的金标准,但WES时间成本和分析成本较高。经过多项大样本研究验证后,TMB检测从WES扩展到了更切合临床实际的靶向二代测序(next-generation sequencing panel, NGS panel)。靶向测序的基因检测位点比外显子组少,由于不同平台检测方法和测序覆盖的外显子区域长度不同,TMB也被定义为肿瘤基因组区域中每兆碱基(megabase, Mb)发生的碱基替换突变和插入缺失突变的数量总和,单位为muts/Mb。,明确说明了时编码区的变异数目,虽然对应区域同理应该选用编码区长度,但是共识未明确体积分母的计算方式。[肿瘤突变负荷检测及临床应用中国专家共识(2020年版)] 中提到
以数百个基因的肿瘤靶向 Panel 检测是通过计算覆盖在产品外显子上的体细胞突变数目除以产品的外显子覆盖区域得到基于 Panel 的 TMB 结果,然而其计算得到的 TMB值与 WES 检测得到的 TMB 值存在偏差,说明了以产品的外显子覆盖区域作为分母。[TMB标准化项目蓝皮书]在中检院组织的TMB标准化项目中,针对WES的计算提供了分母的计算方式
位于全外显子捕获区间区域上下游扩展50bp 与 CDS 区域上下游扩展 2bp 的交集区域。,分母对应的范围时CDS区域上方下游2bp区域。
其实目前国内大部分检测公司并没有开展临床试验,而目前评估Panel的性能也多为和WES结果进行相关性比较,但是显然,分母作为一个常数值,不管如何选择,都不会影响相同计算体系下的样本排序。以下是一些国际检测产品的计算方式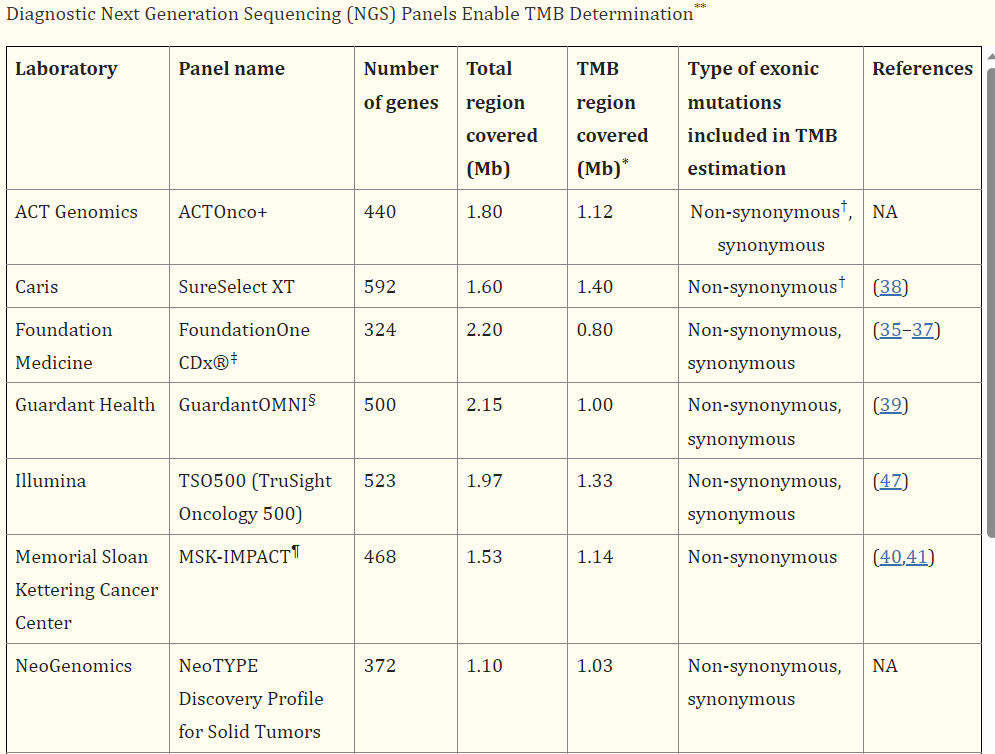
Panel大小
有一些证据[23,24]发现检测的基因数越多,TMB的检测结果与WES的一致性越高,NGS大panel可能更适合评估TMB。对于TMB较高的样本,不同大小的NGS panel检测结果差异可能不显著;而对于TMB较低的样本,检测结果的不一致性显著增加。目前一般认为NGS panel ≥0.8 Mb可以较好地评估肿瘤组织TMB水平(Implementing TMB measurement in clinical practice: considerations on assay requirements)。
参考材料: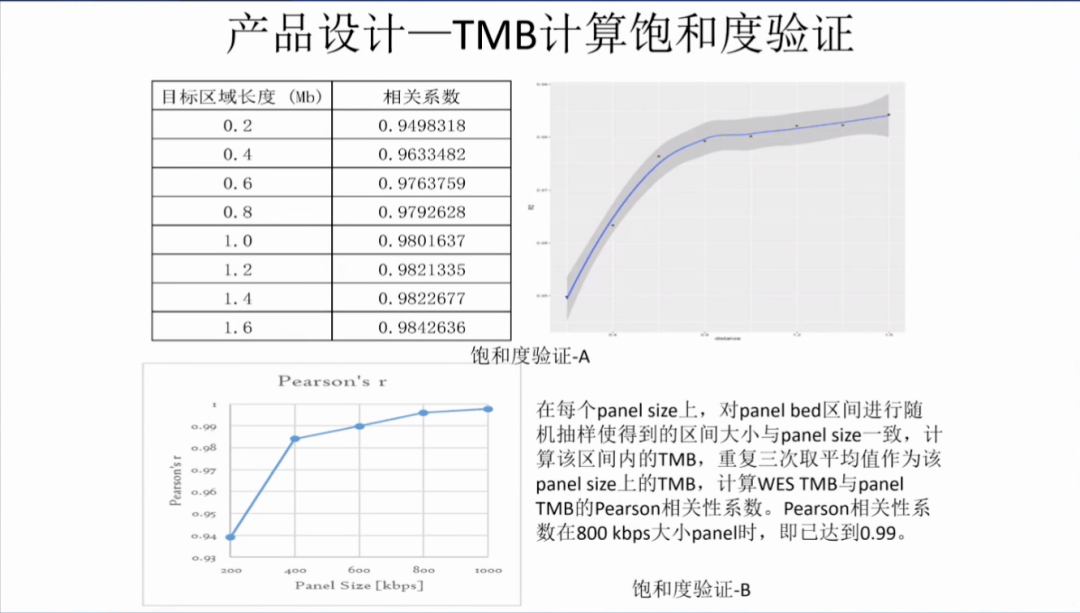
来源:历史中检院宣讲PPT材料
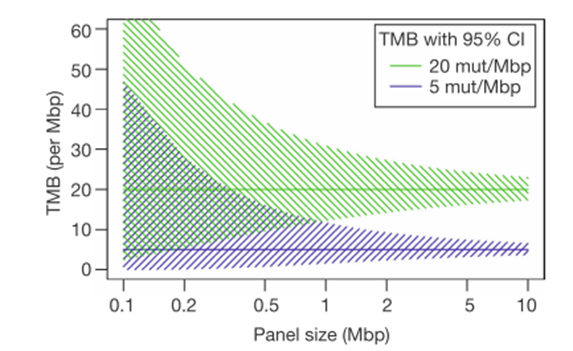
Transl Lung Cancer Res 2018;7(6):703-715
Genes Chromosomes Cancer. 2019;58:578–588.
影响因素
样本收集阶段、DNA处理阶段、测序阶段、生物信息分析阶段和报告生成阶段均会影响TMB检测的可靠性。样本收集阶段主要包括样本类型、肿瘤类型、肿瘤异质性和克隆进化等影响因素;DNA处理阶段包括DNA质量和数量、文库构建等影响因素;测序阶段包括DNA捕获区域、测序深度、覆盖读长、测序平台等影响因素;生物信息分析阶段包括突变类型、胚系突变过滤、等位基因突变频率等影响因素;报告生成阶段包括瘤种分类、患者人群、患者数量、TMB排序标准等影响因素。除了考虑技术因素,流程监管、样本收集和处理质控以及样本运送时长等因素可能也会影响样本质量,从而影响检测结果。
关联指标
在一定程度上,TMB 水平反映的是肿瘤细胞内DNA 的修复损伤情况,与产生肿瘤新抗原能力密切相关。DNA错配修复基因(mismatch repair genes,MMR)负责修正DNA 复制错误,若MMR 存在突变往往会导致微卫星不稳定(microsatellite instability,MSI),因此高微卫星不稳定(MSI high,MSI鄄H)常作为MMR 功能缺陷(mismatch repair deficient,dMMR)的替代指标[6]。
此外,DNA 聚合酶着(DNA polymerase 着,POLE)和DNA 聚合酶啄1(polymerase delta 1,POLD1)对DNA复制的校对和保真至关重要,POLE/POLD1 基因突变(特别是外切酶活性域突变)也会导致肿瘤的高突变或超突变(TMB>100 个突变/Mb)(Tumor and Microenvironment Evolution during Immunotherapy with Nivolumab)
TMB发展重要节点历程
TMB概念起源于2013年Nature发表的一项研究(Signatures of mutational processes in human cancer)。在30个癌种7,000多个标本中,研究者通过全基因组测序(whole genome sequencing,WGS)和全外显子测序(whole exome sequencing, WES)技术分析了突变图谱,描述了不同癌种样本中每百万碱基(megabase, Mb)的突变数量。
2014年的一项黑色素瘤研究(Genetic Basis for Clinical Response to CTLA-4 Blockade in Melanoma)发现,免疫治疗的响应率与肿瘤突变数目有一定的相关性,通过WES检出错义突变数量大于100的患者接受免疫治疗后具有更长的总生存期(overall survival, OS),这是首个验证TMB和免疫治疗疗效相关性的研究。
2015年,首个TMB与NSCLC免疫治疗疗效的研究(Mutational landscape determines sensitivity to PD-1 blockade in non–small cell lung cancer)发表于Science,该研究发现高于中位TMB的NSCLC患者具有更长的无进展生存期(progression-free survival, PFS)。
此后,CheckMate-026、CheckMate-227等多项大型研究证实了TMB对NSCLC免疫治疗疗效的预测作用。
2017年,Genome Medicine发表的一项10万例实体瘤患者研究(Analysis of 100,000 human cancer genomes reveals the landscape of tumor mutational burden),探索了靶向捕获测序panel与WES检测TMB的相关性,证实了panel检测TMB的可行性与可靠性。
2019年中国临床肿瘤学会(Chinese Society of Clinical Oncology, CSCO)指南和美国国家综合癌症网络(National Comprehensive Cancer Network, NCCN)指南均将TMB纳入晚期肺癌的分子病理检测范围。
2020年,美国食品药品监督管理局(Food and Drug Administration, FDA)批准Pembrolizumab单药用于治疗高TMB且既往接受治疗后病情进展的不可手术或转移性实体瘤患者。Pembrolizumab成为全球首个以TMB作为标志物而获批的抗肿瘤药物。但临床实践中TMB的检测和评估缺乏统一的标准,这极大限制了其临床应用。虽然《肿瘤突变负荷检测及临床应用中国专家共识(2020年版)》已发布,但TMB在肺癌免疫治疗临床应用中的相关规范仍有待统一。
2021年,为促进TMB在肺癌免疫治疗中应用的规范化,协作组组织国内肺癌领域权威专家,综合国内外高质量文献,形成《肿瘤突变负荷应用于肺癌免疫治疗的专家共识》,对TMB的定义、临床意义和临床应用给出指导性建议。
TMB 重要资讯
TMB是肿瘤NGS检测
TMB相关文章指南共识信息
| 发布时间 | 简介 | 机构 | 文章材料 |
|---|---|---|---|
| 2019.10.17 | 肿瘤突变负荷检测国家参考品说明书公示 | 中检院 | 肿瘤突变负荷检测国家参考品说明书公示 |
| 2020.06 | 肿瘤突变负荷检测国家参考品 | 中检院 | 肿瘤突变负荷检测国家参考品 |
| 2020.10 | 肿瘤突变负荷检测及临床应用中国专家共识(2020 年版) | 中国癌症防治杂志 | 肿瘤突变负荷检测及临床应用中国专家共识(2020年版) |
| 2021.11 | TMB国内共识 - 面向肺癌 | 中国临床肿瘤学会 | 肿瘤突变负荷应用于肺癌免疫治疗的专家共识 |
TMB阈值确定方法
标准化的阈值,应该使用临床疗效数据进行阈值的判断!
目前部分文章是使用的人群比例占比进行的TMB High/Low的划分。
阈值确定参考素材
| index | TMB-High | TMB-intermedia | TMB-L | 参考文献 |
|---|---|---|---|---|
| 1 | Top 10% | Top 10%-20% | else | https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7210182/ |
| 2 | Top 10% | Top 10%-50% | else | https://mct.aacrjournals.org/content/molcanther/16/11/2598.full.pdf |
免疫治疗响应疗效报道
BGI的TMB工作
TMB计算逻辑
1.5% 以上的SNV(含同义突变)和InDel的总突变数目除以芯片大小(2.79M)
其中包含同义突变的参考依据如下:
- Chalmers ZR, et al. Analysis of 100,000 human cancer genomes reveals the landscape of tumor mutational burden. Genome Med. 2017;9:34. doi: 10.1186/s13073-017-0424-2.
- Rosenberg JE, et al. Atezolizumab in patients with locally advanced and metastatic urothelial carcinoma who have progressed following treatment with platinum-based chemotherapy: a single-arm, multicentre, phase 2 trial. Lancet. 2016;387(10031):1909–1920
- Han Chang, Ariella Sasson, Sujaya Srinivasan, Ryan Golhar, Danielle M. Greenawalt, William J. Geese, George Green, Kim Zerba, Stefan Kirov, Joseph Szustakowski bioRxiv 626143; doi: https://doi.org/10.1101/626143
- FM 原文参考: TMB by F1CDx is defined based on counting the total number of all synonymous and non-synonymous variants present at 5% allele frequency or greater (after filtering) and reported as mutations per megabase (mut/Mb) unit. The clinical validity of TMB defined by this panel has not been established
TMB标准化项目
整体时间规划
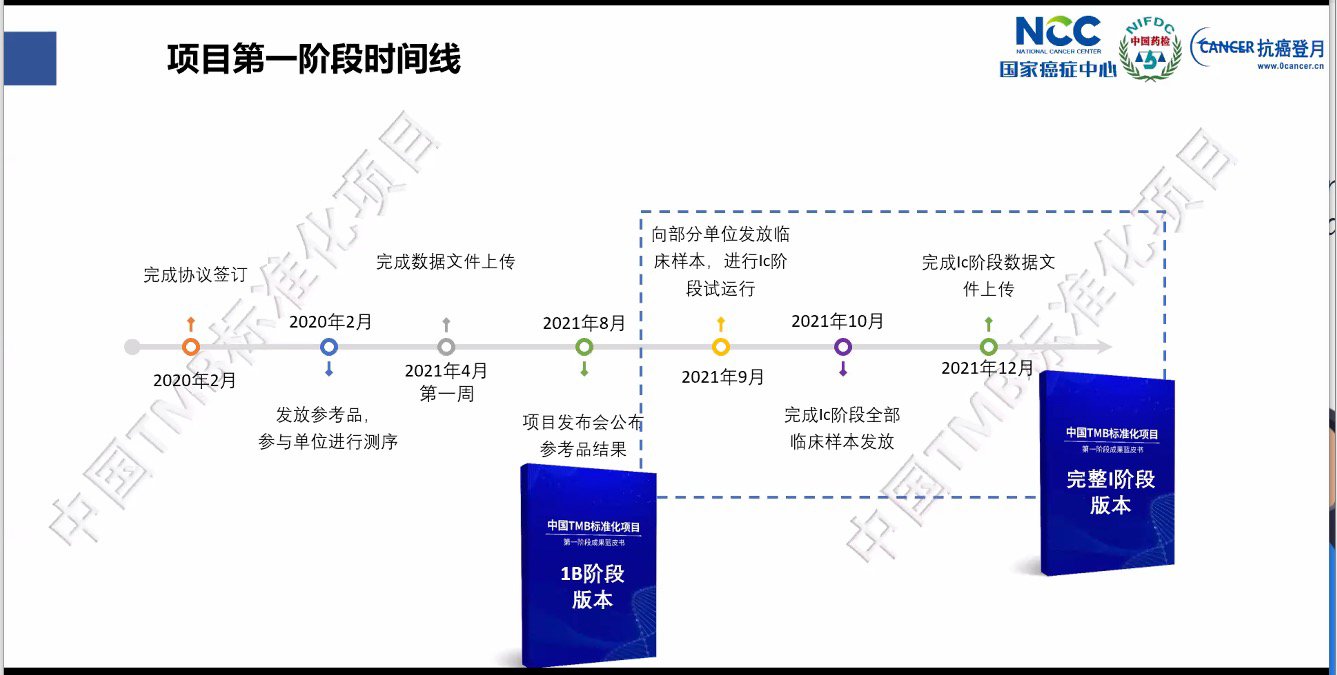
第一阶段结果
基于华大数据进行Panel和WES的相关性拟合
基于TCGA公共数据,进行拟合,获取各公司Panel计算TMB值和原WES水平TMB的回归拟合公式。
y=1.371559x-0.735414 (x:Panel检测的TMB值; y:经过矫正后,对应WES水平的TMB值。)
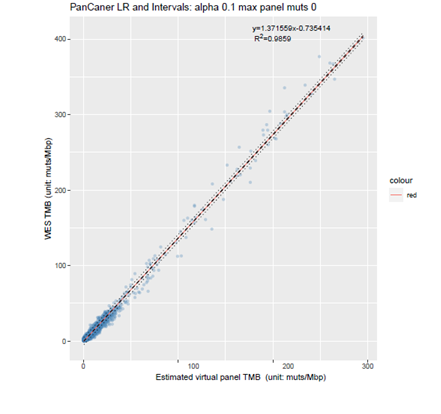
使用该公式,对PanCancer(688芯片)检测临床样本获得的TMB值进行校正,并利用校正后的数据和WES检测TMB结果进行相关性比较,结果如下: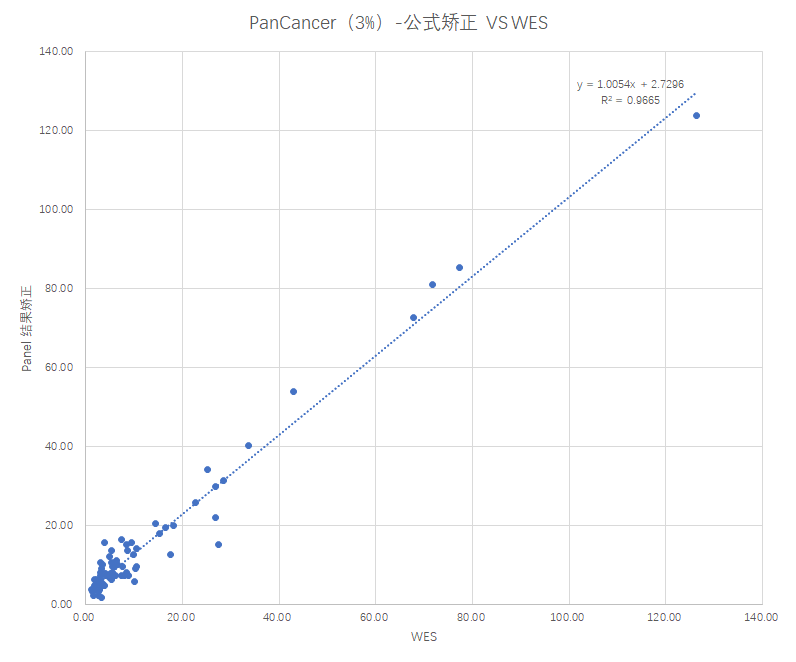
第一阶段总结
华大数据基于三分段确定的阈值
BGI历史数据阈值(三分段)
基于该标准(index1)和华大历史样本确定的整体阈值(数据截止2020.8)
| 癌症类型 | TMB high | TMB median | TMB low |
|---|---|---|---|
| 组织泛癌种 | ≥8.6Mut/Mb | >5.02Mut/Mb且<8.6Mut/Mb | ≤5.02Mut/Mb |
基于该标准(index1)和华大历史样本确定的各个癌种阈值(数据截止2021.9)
| 癌症类型 | TMB high | TMB median | TMB low |
|---|---|---|---|
| 胆管癌 Cholangiocarcinoma | ≥5.73Mut/Mb | >3.94Mut/Mb且<5.73Mut/Mb | ≤3.94Mut/Mb |
| 胆囊癌 Carcinoma of Gallbladder | ≥8.6Mut/Mb | >4.66Mut/Mb且<8.6Mut/Mb | ≤4.66Mut/Mb |
| 非小细胞肺癌 Non-Small Cell Lung Cancer | ≥9.68Mut/Mb | >6.09Mut/Mb且<9.68Mut/Mb | ≤6.09Mut/Mb |
| 肝细胞癌 Hepatocellular Carcinoma | ≥7.89Mut/Mb | >5.38Mut/Mb且<7.89Mut/Mb | ≤5.38Mut/Mb |
| 宫颈癌 Cervical Cancer | ≥16.49Mut/Mb | >8.96Mut/Mb且<16.49Mut/Mb | ≤8.96Mut/Mb |
| 黑色素瘤 Melanoma | ≥8.24Mut/Mb | >3.94Mut/Mb且<8.24Mut/Mb | ≤3.94Mut/Mb |
| 结直肠癌 Colorectal Cancer | ≥27.24Mut/Mb | >6.45Mut/Mb且<27.24Mut/Mb | ≤6.45Mut/Mb |
| 卵巢癌 Ovarian Cancer | ≥5.73Mut/Mb | >3.94Mut/Mb且<5.73Mut/Mb | ≤3.94Mut/Mb |
| 膀胱癌 Bladder Cancer | ≥20.07Mut/Mb | >10.75Mut/Mb且<20.07Mut/Mb | ≤10.75Mut/Mb |
| 前列腺癌 Prostate Cancer | ≥8.6Mut/Mb | >6.09Mut/Mb且<8.6Mut/Mb | ≤6.09Mut/Mb |
| 乳腺癌 Breast Cancer | ≥6.81Mut/Mb | >5.38Mut/Mb且<6.81Mut/Mb | ≤5.38Mut/Mb |
| 软组织肉瘤 Soft Tissue Sarcoma | ≥4.66Mut/Mb | >2.87Mut/Mb且<4.66Mut/Mb | ≤2.87Mut/Mb |
| 肾癌 Kidney Cancer | ≥6.45Mut/Mb | >3.94Mut/Mb且<6.45Mut/Mb | ≤3.94Mut/Mb |
| 头颈癌 Head and Neck Cancer | ≥8.6Mut/Mb | >5.73Mut/Mb且<8.6Mut/Mb | ≤5.73Mut/Mb |
| 胃癌 Gastric Cancer | ≥12.19Mut/Mb | >7.17Mut/Mb且<12.19Mut/Mb | ≤7.17Mut/Mb |
| 胰腺癌 Pancreatic Adenocarcinoma | ≥3.94Mut/Mb | >2.51Mut/Mb且<3.94Mut/Mb | ≤2.51Mut/Mb |
| 子宫肿瘤 Uterine Neoplasms | ≥26.88Mut/Mb | >17.92Mut/Mb且<26.88Mut/Mb | ≤17.92Mut/Mb |
基于该标准(index1)和华大历史样本确定的各个癌种阈值(数据截止2022.04,质评用)
|癌症类型|TMB high|TMB median|TMB low|
|-|-|-|-|
|泛癌种(15917例)|≥9.68Mut/Mb|>5.73Mut/Mb且<9.68Mut/Mb|≤5.73Mut/Mb|
|肺腺癌(2733例)|≥8.24Mut/Mb|>5.02Mut/Mb且<8.24Mut/Mb|≤5.02Mut/Mb|
|非小细胞肺癌(4249例) |≥10.04Mut/Mb|>6.45Mut/Mb且<10.04Mut/Mb|≤6.45Mut/Mb|